この記事の目次:
1。アミノ酸の発達
2。構造特性
3。化学組成
4.分類
5。合成
6。物理化学的特性
7。毒性
8。抗菌活性
9。レオロジー特性
10。化粧品業界のアプリケーション
11。日常の化粧品のアプリケーション
アミノ酸界面活性剤(AAS)疎水性グループと1つ以上のアミノ酸を組み合わせることにより形成される界面活性剤のクラスです。この場合、アミノ酸は合成またはタンパク質加水分解物または同様の再生可能な源に由来することができます。このペーパーでは、AASで利用可能なほとんどの合成経路の詳細と、溶解度、分散安定性、毒性、生分解性など、最終製品の物理化学的特性に対する異なるルートの影響について説明します。需要の増加に伴う界面活性剤のクラスとして、それらの可変構造によるAASの汎用性は、多くの商業的機会を提供します。
界面活性剤は、界面活性剤、乳化剤、腐食阻害剤、三次油回収剤、医薬品で広く使用されていることを考えると、研究者は界面活性剤に注意を払うことをやめたことはありません。
界面活性剤は、世界中で毎日大量に消費され、水生環境に悪影響を及ぼしている最も代表的な化学製品です。研究では、従来の界面活性剤の広範な使用が環境に悪影響を与える可能性があることが示されています。
今日、非毒性、生分解性、生体適合性は、界面活性剤の有用性とパフォーマンスと同じくらい消費者にとって非常に重要です。
バイオサーファクタントは、環境に優しい持続可能な界面活性剤であり、細菌、真菌、酵母などの微生物によって自然に合成されるか、細胞外に分泌されます。したがって、バイオサーファクタントは、リン脂質、アルキルグリコシド、アシルアミノ酸などの天然の両親媒性構造を模倣するために、分子設計によって調製することもできます。
アミノ酸界面活性剤(AAS)通常、動物または農業由来の原料から生産される典型的な界面活性剤の1つです。過去20年にわたって、AASは、再生可能リソースから合成できるだけでなく、AASが容易に分解され、無害な副産物を持っているために、環境をより安全にするために、科学者から新しい界面活性剤として大きな関心を集めてきました。
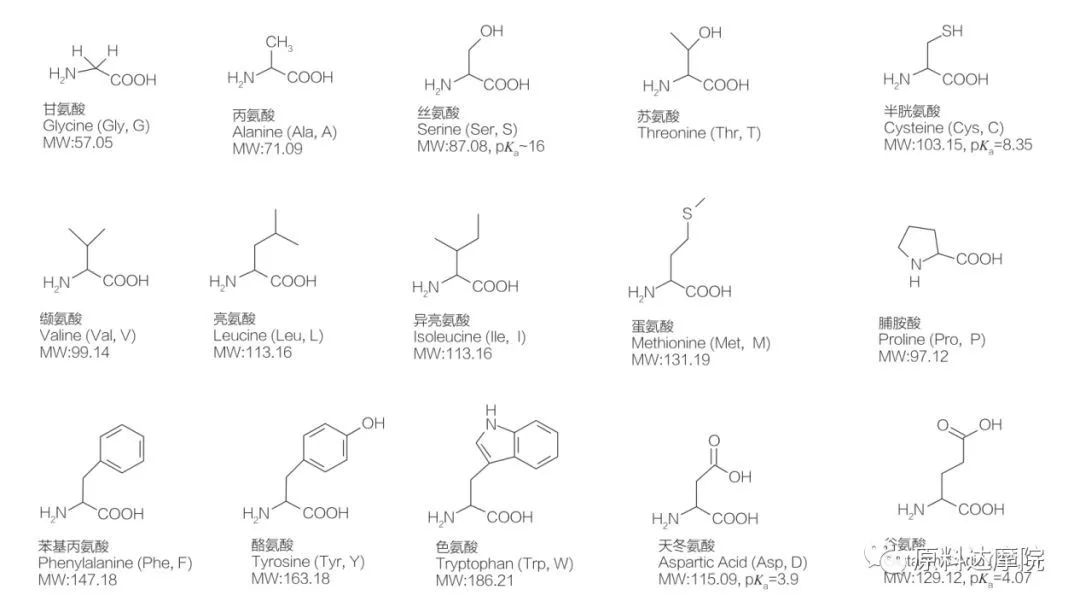
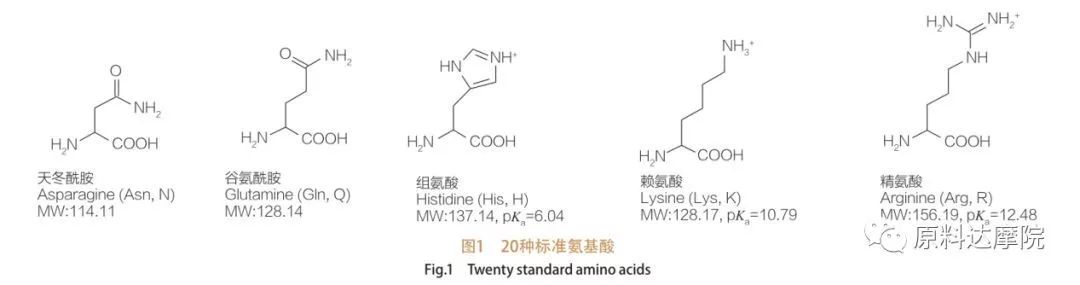
AASは、アミノ酸基(HO 2 C-CHR-NH 2)またはアミノ酸残基(HO 2 C-CHR-NH-)を含むアミノ酸からなる界面活性剤のクラスとして定義できます。アミノ酸の2つの機能領域により、多種多様な界面活性剤の導出が可能になります。合計20の標準的なタンパク質原性アミノ酸が自然に存在することが知られており、成長と生活活動におけるすべての生理学的反応に責任があります。それらは残基Rに従ってのみ互いに異なります(図1、PK Aは溶液の酸解離定数の負の対数です)。一部は極性で疎水性であり、極性で親水性であるものもあり、一部は基本的で、酸性があります。
アミノ酸は再生可能な化合物であるため、アミノ酸から合成された界面活性剤も持続可能で環境に優しい可能性があります。シンプルで自然な構造、低毒性、急速な生分解性により、多くの場合、従来の界面活性剤よりも優れています。再生可能な原料(たとえば、アミノ酸や植物油)を使用して、AASはさまざまなバイオテクノロジールートと化学ルートによって生産できます。
20世紀初頭、アミノ酸は界面活性剤の合成の基質として使用されることが最初に発見されました。AASは、主に医薬品および化粧品の製剤の防腐剤として使用されていました。さらに、AASは、さまざまな疾患を引き起こす細菌、腫瘍、ウイルスに対して生物学的に活性であることがわかりました。 1988年、低コストのAASの可用性により、表面活動に研究対象が生成されました。今日、バイオテクノロジーの開発により、一部のアミノ酸は酵母によって大規模に商業的に合成されることもできます。これは、AASの生産がより環境に優しいことを間接的に証明しています。
01アミノ酸の開発
早くも19世紀初頭、自然に発生するアミノ酸が最初に発見されたとき、それらの構造は非常に価値があると予測されていました - 両親媒性物の調製のための原材料として使用できます。 AASの統合に関する最初の研究は、1909年にBondiによって報告されました。
その研究では、N-アシルグリシンとN-アシルラニンが界面活性剤の親水基として導入されました。その後の研究には、グリシンとアラニンを使用したリポアミン酸(AAS)の合成、およびHentrich et al。一連の調査結果を公開しました最初の特許出願を含む、アシルサルコシン酸塩およびアシルアスパラギン酸塩の使用に関する界面活性剤としての界面活性剤(シャンプー、洗剤、歯磨き粉など)。その後、多くの研究者がアシルアミノ酸の合成と物理化学的特性を調査しました。これまで、AASの統合、特性、産業用途、生分解性に関する多くの文献が発表されています。
02構造特性
AASの非極性疎水性脂肪酸鎖は、構造、鎖の長さ、および数が異なる場合があります。AASの構造的多様性と高い表面活性は、それらの広範な組成の多様性と物理化学的および生物学的特性を説明しています。 AAの頭部は、アミノ酸またはペプチドで構成されています。ヘッドグループの違いは、これらの界面活性剤の吸着、凝集、生物学的活性を決定します。次に、ヘッドグループの官能基は、カチオン性、アニオン性、非イオン性、および両性を含むAAのタイプを決定します。親水性アミノ酸と疎水性の長鎖部分の組み合わせは、分子を表面を非常に活性にする両親媒性構造を形成します。さらに、分子内に非対称炭素原子が存在することは、キラル分子を形成するのに役立ちます。
03化学組成
すべてのペプチドとポリペプチドは、これらの20αタンパク質α-アミノ酸の重合生成物です。 20α-アミノ酸はすべて、カルボン酸官能基(-COOH)とアミノ官能基(-NH 2)を含み、どちらも同じ四面体α炭素原子に付着しています。アミノ酸は、α-炭素に接続された異なるRグループ(Rグループが水素であるLycineを除く)によって互いに異なります。Rグループの構造、サイズ、電荷(酸性度、アルカリ度)が異なる場合があります。これらの違いは、水中のアミノ酸の溶解度も決定します。
アミノ酸はキラル(グリシンを除く)であり、アルファ炭素に関連する4つの異なる置換基を持っているため、自然に光学的に活性です。アミノ酸には2つの可能な立体構造があります。 L-stereoisomersの数が大幅に高いという事実にもかかわらず、それらは互いに重複していない鏡像です。一部のアミノ酸(フェニルアラニン、チロシン、トリプトファン)に存在するRグループはアリールであり、280 nmで最大UV吸収をもたらします。アミノ酸の酸性α-COOHと塩基性α-NH 2はイオン化が可能であり、どちらの立体異性体のいずれにせよ、以下に示すイオン化平衡を構築します。
r-cooh↔r-coo-h+
R-NH3+↔r-nh2h+
上記のイオン化平衡に示されているように、アミノ酸には少なくとも2つの弱酸性基が含まれています。ただし、カルボキシル基はプロトン化アミノ基に比べてはるかに酸性です。 pH 7.4、カルボキシル基は脱プロトン化され、アミノ基はプロトン化されます。非生成不可能なRグループを持つアミノ酸は、このpHで電気的に中性であり、ズウィタリオンを形成します。
04分類
AASは、以下に説明する4つの基準に従って分類できます。
4.1起源に従って
| 起源によれば、AASは次のように2つのカテゴリに分けることができます。 ①自然カテゴリ アミノ酸を含む天然に発生する化合物も、表面/界面張力を低下させる能力を持ち、一部はグリコリピッドの有効性を超えています。これらのAAはリポペプチドとしても知られています。リポペプチドは、通常はバチルス種によって生成される低分子量化合物です。
このようなAAはさらに3つのサブクラスに分割されます。surfactin、iturin、およびfengycin。
|
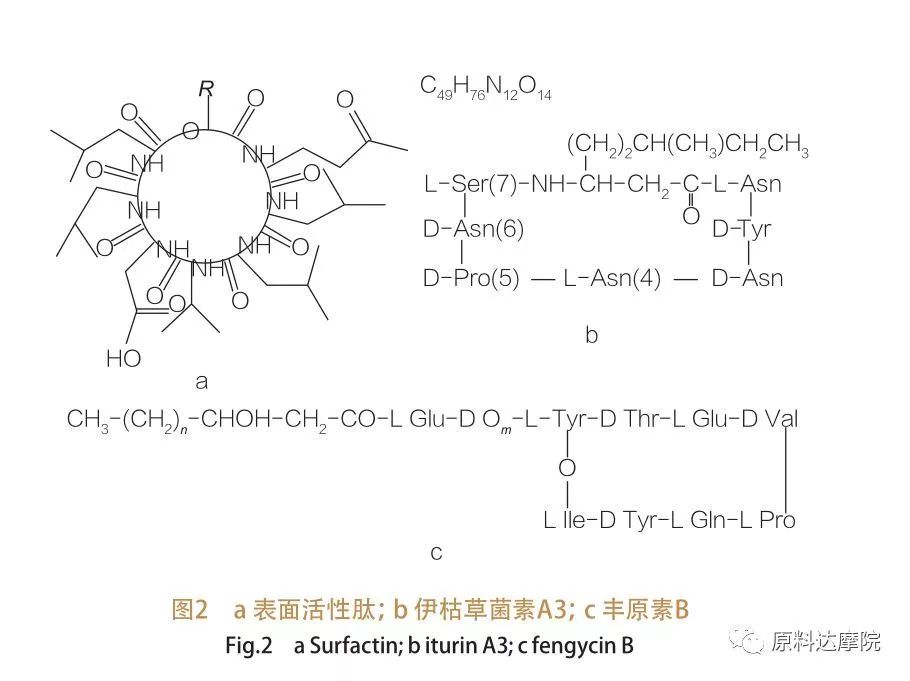
| 表面活性ペプチドのファミリーには、さまざまな物質のヘプタペプチド変異体が含まれます。図2Aに示すように、C12-C16不飽和β-ヒドロキシ脂肪酸鎖がペプチドにリンクされています。表面活性ペプチドは、β-ヒドロキシ脂肪酸のC末端とペプチドの間の触媒により環を閉じている大環性ラクトンです。 Iturinのサブクラスには、6つの主要なバリアント、すなわちIturin AとC、MycosubtilinおよびBacillomycin D、FおよびL.があります。すべての場合において、ヘプタペプチドは、β-アミノ脂肪酸のC14-C17鎖にリンクされています(鎖は多様です)。エクリマイシンの場合、β陽性のアミノ基は、C末端とのアミド結合を形成し、大環状ラクタム構造を形成する可能性があります。
サブクラスのフェンガイシンには、Tyr9がdに設定されている場合にもプリパスタチンとも呼ばれるフェンガイシンAとBが含まれています。デカペプチドは、C14 -C18飽和または不飽和β-ヒドロキシ脂肪酸鎖にリンクされています。構造的に、プリパスタチンはまた、ペプチド配列の位置3にTyr側鎖を含み、C末端残基とのエステル結合を形成し、内部環構造を形成する大環系ラクトンでもある。
②合成カテゴリ AASは、酸性、塩基性、中性アミノ酸のいずれかを使用して合成することもできます。 AASの合成に使用される一般的なアミノ酸は、グルタミン酸、セリン、プロリン、アスパラギン酸、グリシン、アルギニン、アラニン、ロイシン、およびタンパク質加水分解物です。この界面活性剤のサブクラスは、化学、酵素、および化学酵素法によって調製できます。ただし、AASの生産では、化学合成はより経済的に実現可能です。一般的な例には、N-Lauroyl-L-グルタミン酸とN-パルミトイル-L-グルタミン酸が含まれます。
|
4.2脂肪族鎖置換基に基づく
脂肪族鎖の置換基に基づいて、アミノ酸ベースの界面活性剤は2つのタイプに分けることができます。
置換基の位置に応じて
| and-sustituted aas N-置換化合物では、アミノ基が親油性群またはカルボキシル基に置き換えられ、塩基性が失われます。 N-置換AASの最も単純な例は、本質的にアニオン性界面活性剤であるN-アシルアミノ酸です。 N-置換AASには、疎水性および親水性の部分の間にアミド結合が付いています。アミド結合には、酸性環境でのこの界面活性剤の分解を促進する水素結合を形成する能力があり、したがって生分解性になります。
②c-sustituted aas C-置換化合物では、置換はカルボキシル基(アミドまたはエステル結合を介して)で発生します。典型的なC-置換化合物(エステルまたはアミドなど)は、本質的にカチオン性界面活性剤です。
③nおよびc-置換aas このタイプの界面活性剤では、アミノ基とカルボキシル基の両方が親水性の部分です。このタイプは本質的に両性界面活性剤です。 |
4.3疎水性尾の数に従って
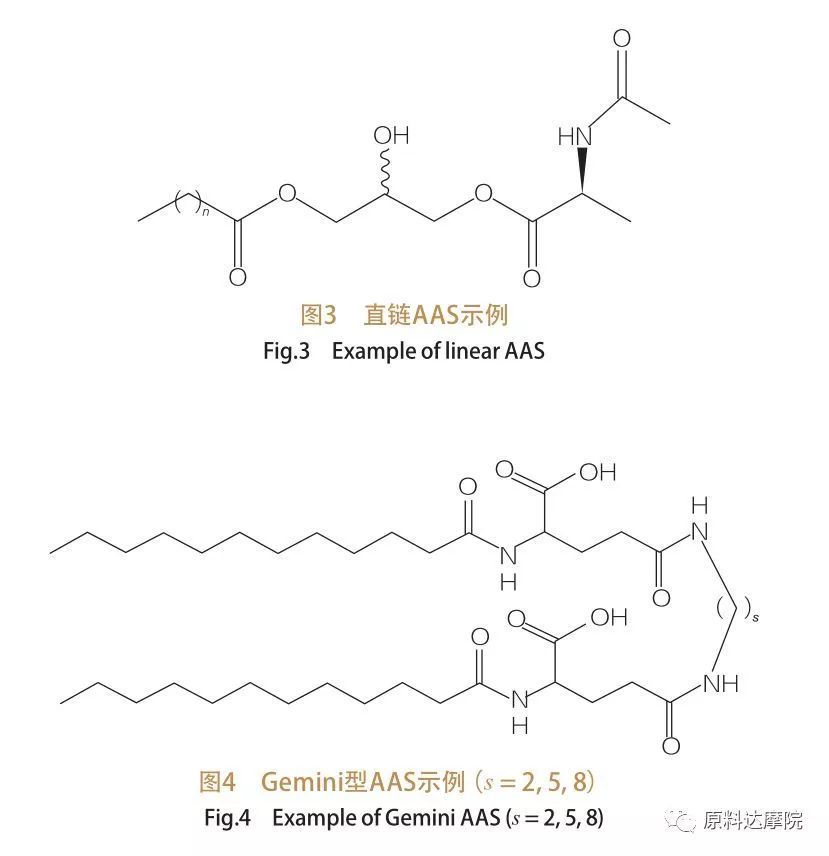
ヘッドグループと疎水性の尾の数に基づいて、AASは4つのグループに分けることができます。ストレートチェーンAAS、ジェミニ(ダイマー)タイプAAS、グリセロリピッド型AAS、およびバイセファリック系両親媒性(BOLA)タイプAAS。ストレートチェーン界面活性剤は、疎水性尾部のみを持つアミノ酸で構成される界面活性剤です(図3)。 Gemini型AAには、分子あたり2つのアミノ酸極ヘッドグループと2つの疎水性尾部があります(図4)。このタイプの構造では、2つのストレートチェーンAAがスペーサーによってリンクされているため、二量体とも呼ばれます。一方、グリセロ脂質タイプAAでは、2つの疎水性尾が同じアミノ酸ヘッドグループに取り付けられています。これらの界面活性剤は、モノグリセリド、ジグリセリド、リン脂質の類似体と見なすことができますが、Bola型AASでは、2つのアミノ酸ヘッドグループが疎水性の尾によってリンクされています。
4.4ヘッドグループのタイプに従って
CATICATIC AAS
このタイプの界面活性剤のヘッドグループは正電荷を持っています。最古のカチオンAASは、エチルココイルアルジン酸であり、これはピロリドンカルボン酸です。この界面活性剤のユニークで多様な特性により、消毒剤、抗菌剤、抗抗剤、ヘアコンディショナー、および目と肌に優しく、生分解性が容易になります。 SingareとMhatreは、アルギニンベースのカチオンAASを合成し、それらの物理化学的特性を評価しました。この研究では、彼らはSchotten-Baumann反応条件を使用して得られた製品の高収量を主張しました。アルキル鎖の長さと疎水性が増加すると、界面活性剤の表面活性が増加し、重要なミセル濃度(CMC)が減少することがわかりました。もう1つは、ヘアケア製品のコンディショナーとして一般的に使用される第四紀アシルタンパク質です。
アニオンAAS
アニオン性界面活性剤では、界面活性剤の極頭群には負の電荷があります。ウニや海の星によく見られるアミノ酸であるサルコシン(CH 3 -NH -CH 2 -COOH、N-メチルグリシン)は、哺乳類細胞に含まれる塩基性アミノ酸であるグリシン(NH 2 -CH 2 -COOH)に化学的に関連しています。 -COOH、)は化学的にグリシンに関連しており、これは哺乳類細胞に見られる塩基性アミノ酸です。ラウリン酸、テトラデカン酸、オレイン酸、およびそのハロゲン化物とエステルは、筋肉の界面活性剤を合成するために一般的に使用されます。サルコシン酸塩は本質的に軽度であるため、うがい薬、シャンプー、スプレーシェービングフォーム、日焼け止め、皮膚クレンザー、その他の化粧品で一般的に使用されています。
その他の市販のアニオンAASには、それぞれAmisoft CS-22およびAmiliteGCK-12が含まれます。これは、それぞれナトリウムnココイル-L-グルタミン酸とカリウムnココイルグリシネートの商品名です。アミライトは、一般的に発泡剤、洗剤、溶解剤、乳化剤、分散剤として使用されており、シャンプー、バス石鹸、ボディウォッシュ、歯磨き粉、フェイシャルクレンザー、クリーンシング石鹸、コンタクトレンズクリーナー、家庭界界などの化粧品に多くの用途があります。 Amisoftは、主にフェイシャルおよびボディクレンザー、合成洗剤、ボディケア製品、シャンプー、その他のスキンケア製品で、マイルドな肌と髪のクレンザーとして使用されています。
③z withericまたは両性AAS
両性界面活性剤には、酸性部位と基本部位の両方が含まれているため、pH値を変更することで電荷を変更できます。アルカリ培地では、アニオン性界面活性剤のように振る舞いますが、酸性環境では、カチオン性界面活性剤のように行動し、両性界面活性剤のような中性培地で行動します。 Lauryl Lysine(LL)およびAlkoxy(2-ヒドロキシプロピル)アルギニンは、アミノ酸に基づく唯一の既知の両性界面活性剤です。 LLは、リジンとラウリン酸の凝縮生成物です。その両性構造により、LLは非常にアルカリ性または酸性溶媒を除いて、ほぼすべてのタイプの溶媒に不溶性です。有機粉末として、LLは親水性表面に優れた接着と摩擦係数が低く、この界面活性剤が優れた優れた潤滑能力を与えます。 LLは、スキンクリームやヘアコンディショナーで広く使用されており、潤滑剤としても使用されています。
④ノニオンAAS
非イオン性界面活性剤は、正式な充電なしで極ヘッドグループによって特徴付けられます。 Al-Sabagh et al。油溶性α-アミノ酸から。このプロセスでは、L-フェニルアラニン(LEP)とL-ロイシンを最初にヘキサデカノールでエステル化し、続いてパルミチン酸との中で、2つのアミドと2つのエステルのα-アミノ酸を与えました。その後、アミドとエステルはエチレンオキシドとの凝縮反応を受けて、異なる数のポリオキシエチレン単位(40、60、100)を持つ3つのフェニルアラニン誘導体を調製しました。これらの非イオン性AAは、良好な洗剤と発泡特性があることがわかりました。
05合成
5.1基本的な合成ルート
AASでは、疎水性基はアミンまたはカルボン酸部位、またはアミノ酸の側鎖を介して付着することができます。これに基づいて、図5に示すように、4つの基本的な合成ルートが利用可能です。
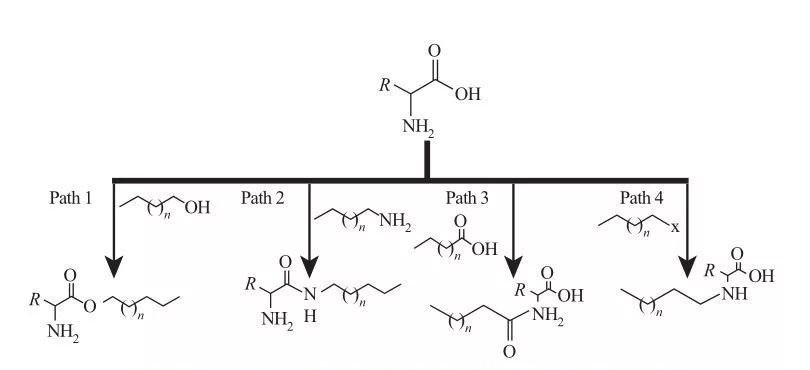
図5アミノ酸ベースの界面活性剤の基本合成経路
| 経路1。 両親媒性エステルアミンは、エステル化反応によって生成されます。この場合、界面活性剤合成は通常、脱水剤と酸性触媒の存在下で脂肪アルコールとアミノ酸を還流することによって達成されます。いくつかの反応では、硫酸は触媒と脱水剤の両方として作用します。
経路2。 活性化アミノ酸はアルキルアミンと反応してアミド結合を形成し、両親媒性アミドアミンの合成をもたらします。
経路3。 アミド酸は、アミノ酸のアミン基をアミド酸と反応させることにより合成されます。
経路4。 長鎖アルキルアミノ酸は、アミン基とハロアルカンの反応によって合成されました。 |
5.2合成と生産の進歩
5.2.1シングルチェーンアミノ酸/ペプチド界面活性剤の合成
N-アシルまたはO-アシルアミノ酸またはペプチドは、脂肪酸を含むアミンまたはヒドロキシル基の酵素触媒アシル化によって合成できます。アミノ酸アミドまたはメチルエステル誘導体の溶媒を含まないリパーゼ触媒合成に関する最も初期の報告は、カンジダ南極を使用し、標的アミノ酸に依存して25%から90%の範囲の収量があります。メチルエチルケトンは、いくつかの反応でも溶媒として使用されています。 Vonderhagen et al。また、水と有機溶媒の混合物(ジメチルホルムアミド/水)とメチルブチルケトンの混合物を使用して、アミノ酸、タンパク質加水分解物および/またはその誘導体のリパーゼおよびプロテアーゼ触媒のN-アシル化反応について説明しました。
初期の頃、AASの酵素触媒合成の主な問題は低収量でした。 Valivety et al。 N-Tetradecanoylアミノ酸誘導体の収率は、異なるリパーゼを使用し、70°Cで何日もインキュベーションした後でも、わずか2%〜10%でした。 Montet et al。また、脂肪酸と植物油を使用したN-アシルリジンの合成におけるアミノ酸の低収量に関する問題にも遭遇しました。彼らによると、製品の最大収量は、溶媒のない条件で19%であり、有機溶媒を使用していました。同じ問題は、Valivetyらによって発生しました。 N-CBZ-L-リジンまたはN-CBZ-リジンメチルエステル誘導体の合成。
この研究では、Nが溶融溶媒を含まない環境の触媒としてNovestected Serineを基質として、Novozyme 435を使用すると、3-O-Tetradecanoyl-L-Serineの収率は80%であると主張しました。ナガオとキトーは、リパーゼを使用すると、リパーゼを使用すると、L-セリン、L-ホモセリン、L-スレオニン、L-チロシン(LET)のOアシル化を研究しました(リパーゼは水性緩衝液培地のカンジダシリンドラ科と根茎デレマールが得られました)。 l-スレオニンと発生した。
多くの研究者は、費用対効果の高いAAの合成のために安価で容易に利用可能な基質の使用をサポートしています。 Soo et al。パーム油ベースの界面活性剤の調製は、固定化されたリポンザイムで最適に機能すると主張しました。彼らは、時間のかかる反応(6日)にもかかわらず、製品の収量はより良くなると指摘しました。ゲロバ等。環状/ラセミ混合物におけるメチオニン、プロリン、ロイシン、スレオニン、フェニルアラニン、フェニルグリシンに基づいたキラルN-パルミトイルAAの合成と表面活性を調査しました。 PangとChuは、溶液中のアミノ酸ベースのモノマーとジカルボン酸ベースのモノマーの合成を、一連の機能的および生分解性アミノ酸ベースのポリアミドエステルを溶液中の共凝縮反応によって合成したことを説明しました。
CantaeuzeneとGuerreiroは、長鎖脂肪族アルコールとジオールを伴うBoc-Ala-OHおよびBoc-ASP-OHのカルボン酸グループのエステル化を報告し、ジクロロメタンは溶媒として、アガロース4B(セファロース4B)を触媒として。この研究では、BOC-ALA-OHと最大16の炭素の脂肪アルコールとの反応は良好な収率(51%)を与えましたが、BOC-ASP-OH 6および12の炭素の場合、対応する収量は63%でした[64]。 99.9%)は、58%から76%の範囲の収率で、パパインが触媒として作用したCBZ-ARG-OMEによるさまざまな長鎖アルキルアミンとのアミド結合またはエステル結合によって合成されました。
5.2.2ジェミニベースのアミノ酸/ペプチド界面活性剤の合成
アミノ酸ベースのジェミニ界面活性剤は、スペーサーグループによって互いに頭と互いに結合する2つの直線鎖AAS分子で構成されています。ジェミニ型アミノ酸ベースの界面活性剤の化学酵素合成には2つの考えられるスキームがあります(図6および7)。図6では、2つのアミノ酸誘導体がスペーサーグループとして化合物と反応し、2つの疎水グループが導入されます。図7では、2つのストレートチェーン構造が二機能性のスペーサーグループによって直接リンクされています。
ジェミニリポアミノ酸の酵素触媒合成の初期の発達は、Valivety et al。吉村等。シスチンおよびN-アルキルブロマイドに基づくアミノ酸ベースのジェミニ界面活性剤の合成、吸着、凝集を調査しました。合成された界面活性剤を、対応するモノマー界面活性剤と比較しました。 Faustino et al。 L-シスチン、D-シスチン、DL-シスチン、L-システイン、L-メチオニン、L-スルホアラニンに基づいたアニオン性尿素ベースのモノマーAAの合成と、それらの導電率、平衡表面張力、定常状態の蛍光特性によるジェミニのペアを説明しました。ジェミニのCMC値は、モノマーとジェミニを比較することにより低いことが示されました。
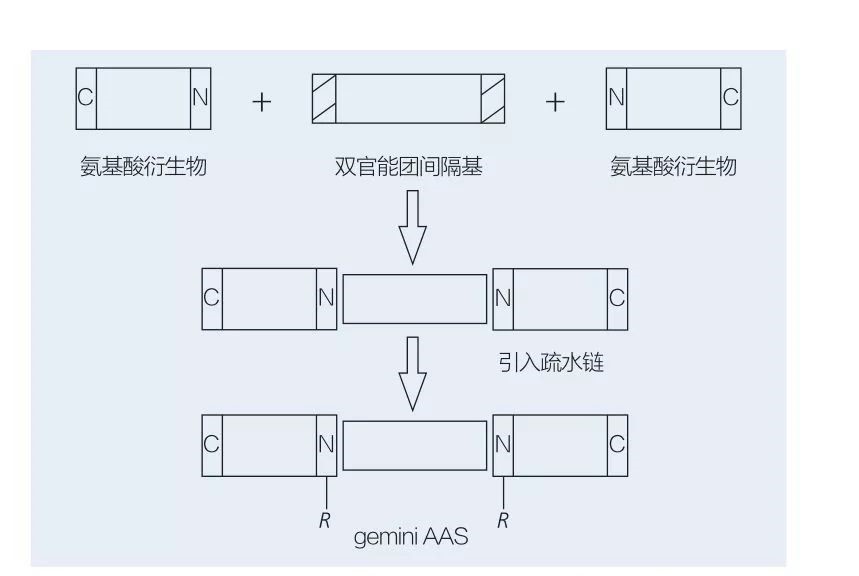
図6 AA誘導体とスペーサーを使用したジェミニAAの合成に続いて、疎水性グループの挿入が続きます
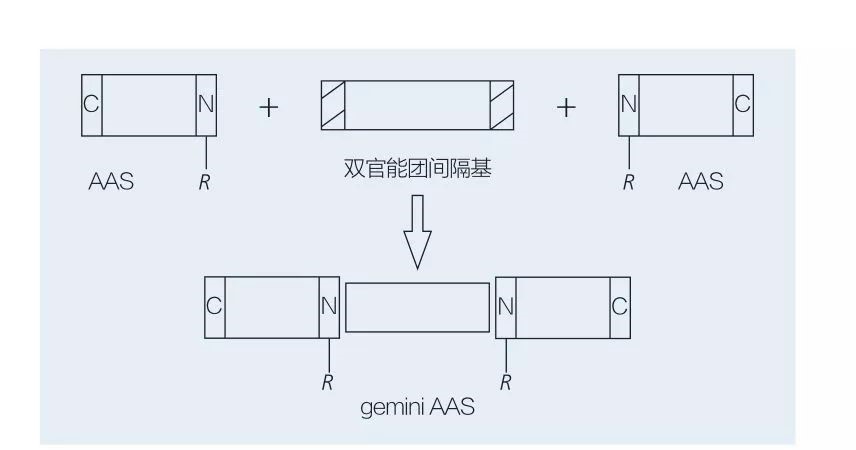
図7二機能スペーサーとAASを使用したジェミニAASSの合成
5.2.3グリセロ脂質アミノ酸/ペプチド界面活性剤の合成
グリセロリピッドアミノ酸/ペプチド界面活性剤は、グリセロールモノ(またはdi-)エステルとリン脂質の構造類似体である脂質アミノ酸の新しいクラスであり、1つまたは2つの脂肪鎖の構造がエステルの結合によりグリセロールバックボーンに関連する1つまたは2つの脂肪鎖の構造です。これらの界面活性剤の合成は、高温および酸性触媒の存在下でのアミノ酸のグリセロールエステルの調製から始まります(例:BF 3)。酵素触媒合成(触媒としてヒドロラーゼ、プロテアーゼ、リパーゼを使用)も良い選択肢です(図8)。
パパインを使用したディラウリル化アルギニングリセリドコンジュゲートの酵素触媒合成が報告されています。アセチルアルギニンからのジアシルグリセロールエステルコンジュゲートの合成とその物理化学的特性の評価も報告されています。
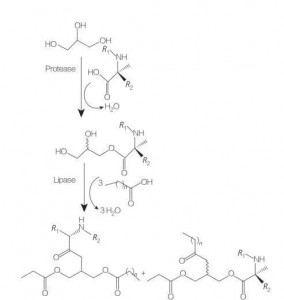
図8モノおよびジアシルグリセロールアミノ酸コンジュゲートの合成
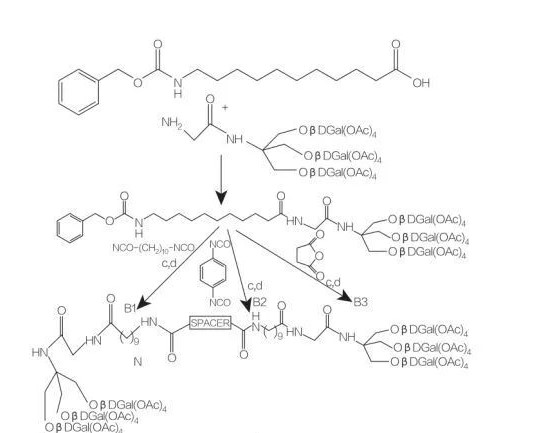
スペーサー:nh-(ch2)10-NH:化合物B1
スペーサー:NH-C6H4-NH:化合物B2
スペーサー:ch2-ch2:化合物B3
図9トリス(ヒドロキシメチル)アミノメタンに由来する対称両親媒性物質の合成
5.2.4 BOLAベースのアミノ酸/ペプチド界面活性剤の合成
アミノ酸ベースのボラ型両親媒性物質には、同じ疎水性鎖に関連する2つのアミノ酸が含まれています。 Franceschi et al。 2つのアミノ酸(D-またはL-アラニンまたはL-ヒスチジン)と異なる長さの1つのアルキル鎖を含むBola型両親媒性物質の合成を説明し、表面活性を調査しました。彼らは、新規Bola型両親媒性物質の合成と凝集を、アミノ酸画分(珍しいβ-アミノ酸またはアルコールのいずれかを使用)とC12 -C20スペーサー基を伴う凝集について議論します。使用される珍しいβ-アミノ酸は、糖アミノシド、アジドチミン(AZT)由来のアミノ酸、ノルボルネンアミノ酸、およびAZTに由来するアミノアルコールである可能性があります(図9)。トリス(ヒドロキシメチル)アミノメタン(TRIS)に由来する対称ボラ型両親媒性物質の合成(図9)。
06 物理化学的特性
アミノ酸ベースの界面活性剤(AAS)は、本質的に多様で汎用性が高く、良好な溶解、良好な乳化特性、高効率、高い表面活性性能、硬水に対する良好な耐性など、多くの用途に良い適用性を持っていることがよく知られています(カルシウムイオン耐性)。
アミノ酸の界面活性剤特性(表面張力、CMC、位相挙動、Krafft温度)に基づいて、広範な研究の後に次の結論に達しました - AASの表面活性は、従来の界面活性剤の対応物の表面活性よりも優れています。
6.1重要なミセル濃度(CMC)
重要なミセル濃度は、界面活性剤の重要なパラメーターの1つであり、溶解、細胞溶解、バイオフィルムとの相互作用などの多くの表面活性特性を管理します。一般に、炭化水素尾の鎖長(疎水性の増加)が増加し、したがって界面活性のCMC値の減少をもたらします。アミノ酸に基づく界面活性剤は、通常、従来の界面活性剤と比較してCMC値が低くなっています。
ヘッドグループと疎水性尾部のさまざまな組み合わせ(モノカチオン性アミド、双方向アミド、二分子アミドベースのエステル)、Infante et al。 3つのアルギニンベースのAASを合成し、CMCとγCMC(CMCでの表面張力)を研究し、CMCとγCMCの値が疎水性尾部の長さの増加とともに減少したことを示しました。別の研究では、SingareとMhatreは、N-α-アシルギニン界面活性剤のCMCが減少し、疎水性尾炭素原子の数が増加することを発見しました(表1)。
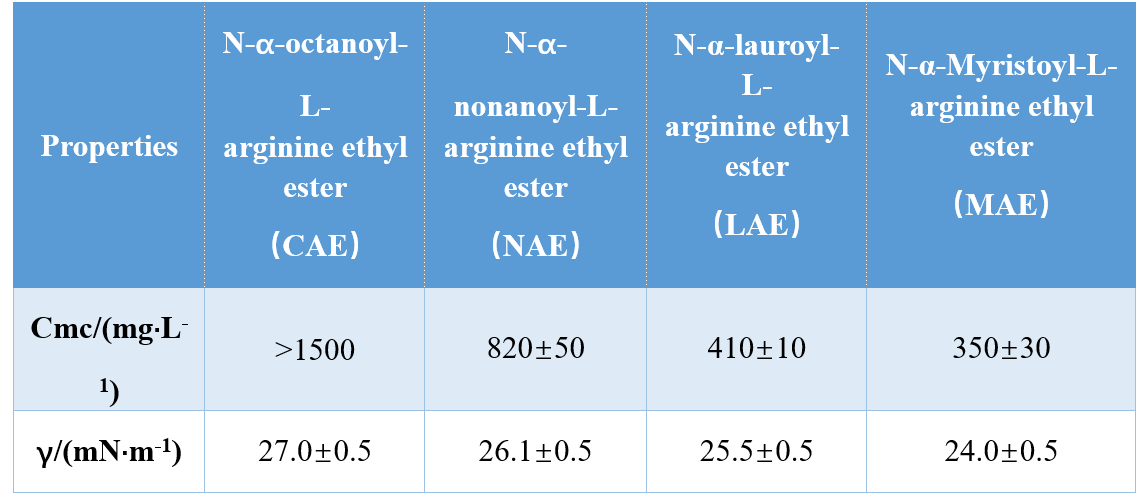
吉村等。システイン由来のアミノ酸ベースのジェミニ界面活性剤のCMCを調査し、疎水性鎖の炭素鎖長が10から12に増加するとCMCが減少することを示しました。炭素鎖の長さをさらに14に増加させると、長鎖ジェミニ界面性があることを確認しました。
Faustino et al。シスチンに基づくアニオン性ジェミニ界面活性剤の水溶液中の混合ミセルの形成を報告しました。ジェミニ界面活性剤は、対応する従来の単量体界面活性剤(C 8 Cys)とも比較されました。脂質界面活性剤混合物のCMC値は、純粋な界面活性剤のCMC値よりも低いと報告されていました。ゲミニ界面活性剤と1,2-ジヘプタノイル-Sn-グリセリル-3-ホスホコリンは、水溶性のミセル形成リン脂質であり、CMCをミリモルレベルで持っていました。
シュレスタとアラマキは、混合塩の非存在下での混合アミノ酸ベースのアニオン性ニオン性界面活性剤の水溶液中の粘弾性ワーム様ミセルの形成を調査しました。この研究では、N-ドデシルグルタミン酸はKrafft温度が高いことがわかりました。しかし、塩基性アミノ酸L-リジンで中和すると、ミセルが生成され、溶液は25°Cでニュートン液のように動作し始めました。
6.2良好な水溶解度
AASの良好な水溶解度は、追加のCO-NH結合の存在によるものです。これにより、AASは、対応する従来の界面活性剤よりも生分解性で環境に優しいものになります。 N-アシル-L-グルタミン酸の水溶解度は、その2つのカルボキシル基のためにさらに優れています。 CN(CA)2の水溶解度も良好であり、1分子に2つのイオンアルギニン基があるため、細胞界面でのより効果的な吸着と拡散、さらには低濃度での効果的な細菌阻害さえもなります。
6.3 Krafft温度とKrafftポイント
Krafft温度は、溶解度が特定の温度を急激に増加させる界面活性剤の特定の溶解度挙動として理解できます。イオン性界面活性剤は、固体水和物を生成する傾向があり、水から沈殿する可能性があります。特定の温度(いわゆるKrafft温度)では、通常、界面活性剤の溶解度の劇的で不連続な増加が観察されます。イオン界面活性剤のKrafft点は、CMCのKrafft温度です。
この溶解度特性は通常、イオン界面活性剤で見られ、次のように説明できます。界面活性剤を含まないモノマーの溶解度は、Krafftポイントに到達するまでKrafft温度を下回り、ミセル形成により溶解度が徐々に増加します。完全な溶解度を確保するには、Krafftポイントより上の温度で界面活性剤製剤を準備する必要があります。
AASのKrafft温度が研究され、従来の合成界面活性剤の温度と比較されています。シュレスタとアラマキは、アルギニンベースのAAのKrafft温度を研究し、重要なミセル濃度が2-5×10-6モル-L -1を超えるnet eet formation(ohtel formation(sine sinter sinter)を伴う2-5×10-6 mol-l -1を超える凝集挙動を示すことがわかりました。 AASと、Krafft温度とアミノ酸残基の関係について議論しました。
実験では、n-ヘキサデカノイルAAのKrafft温度は、アミノ酸残基のサイズの減少とともに増加することがわかりました(フェニルアラニンは例外です)が、溶解度の熱(熱中)はアミノ酸残基のサイズの減少とともに増加しました(グリシンとフェニルアラニンを除く)。アラニンおよびフェニルアラニン系の両方で、DL相互作用は、N-ヘキサデカノイルAAS塩の固体形態でのLL相互作用よりも強いと結論付けられました。
Brito et al。差動スキャン微量回体量測定を使用して、3つのシリーズの新規アミノ酸ベースの界面活性剤のKrafft温度を決定し、トリフルオロアセテートイオンをヨウ化イオンに変更すると、47°Cから53°Cにkrafft温度(約6°C)が大幅に増加することがわかりました。シスダブル結合の存在と、長鎖の介入に存在する不飽和により、Krafft温度が大幅に低下しました。 N-ドデシルグルタミン酸は、Krafft温度が高いことが報告されています。しかし、塩基性アミノ酸L-リジンによる中和により、溶液中のミセルが25°Cでニュートン液のように振る舞うことをもたらしました。
6.4表面張力
界面活性剤の表面張力は、疎水性部分の鎖長に関連しています。 Zhang et al。ウィルヘルミープレート法(25±0.2)°Cにより、ココイルグリシネートナトリウムの表面張力を決定し、CMCの表面張力値を33 mn -M -1、CMCとして0.21 mmol -L -1として決定しました。吉村等。 2c n cysタイプのアミノ酸ベースの表面張力2c n cysベースの表面張力の表面張力を決定しました。 CMCでの表面張力は、鎖の長さが増加すると(n = 8まで)減少し、n = 12以下の鎖長の界面活性剤では傾向が逆転したことがわかりました。
ジカルボキシル化アミノ酸ベースの界面活性剤の表面張力に対するCAC1 2の効果も研究されています。これらの研究では、CAC1 2を3つのジカルボキシル化アミノ酸型界面活性剤(C12 MALNA 2、C12 ASPNA 2、およびC12 Gluna 2)の水溶液に添加しました。 CMC後のプラトー値を比較し、非常に低いCAC1 2濃度で表面張力が減少することがわかりました。これは、ガス水界面での界面活性剤の配置に対するカルシウムイオンの影響によるものです。一方、N-ドデシルアミノマノマン酸およびN-ドデシルアスパラギン酸の塩の表面緊張も、最大10 mmol-L -1 Cac1 2濃度までほぼ一定でした。 10 mmol -L -1を超えると、界面活性剤のカルシウム塩の沈殿の形成により、表面の張力が急激に増加します。 n-ドデシルグルタミン酸の二部塩の場合、CAC1 2の中程度の添加は表面張力の有意な減少をもたらし、CAC1 2濃度の継続的な増加はもはや有意な変化を引き起こしませんでした。
ガス水界面でのジェミニ型AASの吸着速度論を決定するために、最大バブル圧力法を使用して動的な表面張力を決定しました。結果は、最も長いテスト時間で、2C 12 Cys動的表面張力が変化しなかったことを示しました。動的な表面張力の減少は、濃度、疎水性尾の長さ、および疎水性尾の数にのみ依存します。界面活性剤の濃度の増加、鎖の長さの減少、および鎖の数は、より急速な減衰をもたらしました。より高い濃度のC n Cys(n = 8〜12)で得られた結果は、ウィルヘルミー法で測定されたγCMCに非常に近いことがわかりました。
別の研究では、ディラウリルシスチンナトリウム(SDLC)とディデカミノナトリウムシスチンの動的表面張力は、ウィルヘルミープレート法によって決定され、さらに、それらの水溶液の平衡表面張力は、液滴法によって決定されました。ジスルフィド結合の反応は、他の方法でもさらに調査されました。 0.1 mmol -L -1SDLC溶液にメルカプトエタノールを添加すると、表面張力が34 MN -M -1から53 MN -M -1に急速に増加しました。 NaCloはSDLCのジスルフィド結合をスルホン酸基に酸化できるため、Naclo(5 mmol -L -1)を0.1 mmol -L -1 SDLC溶液に加えた場合、凝集体は観察されませんでした。透過型電子顕微鏡と動的光散乱の結果は、溶液に凝集体が形成されていないことを示しました。 SDLCの表面張力は、20分間で34 MN -M -1から60 MN -M -1に増加することがわかりました。
6.5バイナリ表面相互作用
ライフサイエンスでは、多くのグループがカチオン性AAS(ジアシルグリセロールアルギニンベースの界面活性剤)の混合物の振動特性を研究し、ガス水界面でリン脂質を研究しており、最終的にこの非理論的特性は静電相互作用の有病率を引き起こすと結論付けています。
6.6集約プロパティ
動的光散乱は、CMCを超える濃度でアミノ酸ベースのモノマーとジェミニ界面活性剤の凝集特性を決定するために一般的に使用され、見かけの流体力学的直径DH(= 2R H)を生成します。 C n Cysと2CN Cysによって形成される凝集体は比較的大きく、他の界面活性剤と比較して大規模な分布を持っています。 2C 12 Cysを除くすべての界面活性剤は、通常、約10 nmの凝集体を形成します。ジェミニ界面活性剤のミセルサイズは、モノマーの対応物のサイズよりも大幅に大きいです。炭化水素鎖の長さの増加は、ミセルサイズの増加にもつながります。 Ohta et al。水溶液中のN-ドデシル - フェニル - アラニル - フェニル - フェニル - アラニンテトラメチルアンモニウムの3つの異なるステレオ異性体の凝集特性を説明し、ジアステレオ異性体が水性溶液に同じ臨界凝集濃度を持っていることを示しました。岩山等循環二色性、NMR、および蒸気圧液測定により調査されたN-ドデカノイル-L-グルタミン酸、N-ドデカノイル-L-バリン、およびそのメチルエステルのキラル凝集体の形成(異なる溶媒)循環二色性、NMRおよび蒸気圧浸透圧。
6.7界面吸着
アミノ酸ベースの界面活性剤の界面吸着とその従来の対応物との比較も、研究方向の1つです。たとえば、LETとLEPから得られた芳香族アミノ酸のドデシルエステルの界面吸着特性を調査しました。結果は、LETとLEPがそれぞれガス液体界面と水/ヘキサン界面でより低い界面領域を示したことを示しました。
Bordes et al。 3つのジカルボキシル化アミノ酸界面活性剤、ドデシルグルタミン酸、ドデシルアスパラギン酸、およびアミノマロネートの二dis部の塩(それぞれ2つのカルボキシル基の間の3、2、および1つの炭素原子)のガス水界面での溶液挙動と吸着を調査しました。このレポートによると、ジカルボキシル化界面活性剤のCMCは、モノカルボキシル化ドデシルグリシン塩のCMCよりも4〜5倍高かった。これは、その中のアミド基を介したジカルボキシル化界面活性剤と隣接する分子との間の水素結合の形成に起因します。
6.8位相動作
等方性の不連続な立方相は、非常に高い濃度の界面活性剤で観察されます。非常に大きな頭群を持つ界面活性剤分子は、より小さな正の曲率の凝集体を形成する傾向があります。 Marques et al。 12Lys12/12serおよび8Lys8/16Serシステムの位相挙動を研究し(図10を参照)、結果は12Lys12/12serシステムがミセル溶液領域と小胞溶液領域の間に位相分離ゾーンを持っている一方で、8Lys8/16Serシステムは8LyS8/16SERシステムが微微量透過性と小孔の間で微微量微細症の間で微微量膜領域に至ると、極地の間で微微量透過性を示していることを示しました。 地域)。 12lys12/12serシステムの小胞領域では、小胞は常にミセルと共存しているが、8Lys8/16serシステムの小胞領域には小胞のみがあることに注意する必要があります。
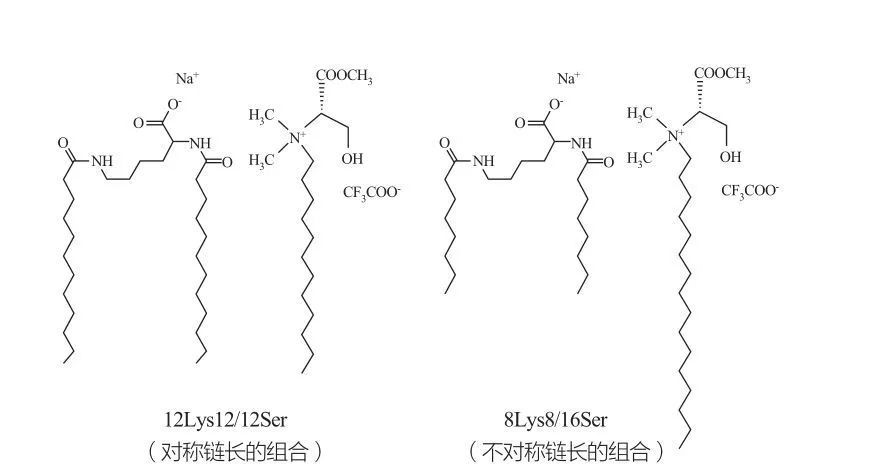
リジンおよびセリンベースの界面活性剤のカタニオン性混合物:対称12lys12/12serペア(左)および非対称8Lys8/16serペア(右)
6.9乳化能力
大上等n- [3-ドデシル-2-ヒドロキシプロピル] -l-アルギニン、L-グルタミン酸、およびその他のAAの乳化能力、界面張力、分散性、および粘度を調べました。合成界面活性剤(従来の非イオン性および両性対応)と比較して、結果は、AASが従来の界面活性剤よりも強い乳化能力を持っていることを示しました。
Baczko et al。合成された新規アニオン性アミノ酸界面活性剤を合成し、キラル指向NMR分光法溶媒としての適合性を調査しました。異なる疎水性尾部(ペンチル〜テトラデシル)を持つ一連のスルホン酸ベースの両親媒性L-PHEまたはL-ALA誘導体は、Aアミノ酸をO-スルホベンゾティックアニドリドと反応させることにより合成されました。 Wu et al。 N-FattyアシルAAの合成されたナトリウム塩と水中乳剤の乳化能力を調査し、その結果、これらの界面活性剤は、油相としてのn-ヘキサンよりも油相として酢酸エチルで優れていることが示されました。
6.10合成と生産の進歩
硬い耐水性は、硬水中のカルシウムやマグネシウムなどのイオンの存在に抵抗する界面活性剤の能力、つまりカルシウム石鹸への沈殿を避ける能力として理解できます。硬い耐水性が高い界面活性剤は、洗剤の製剤やパーソナルケア製品に非常に役立ちます。カルシウムイオンの存在下での界面活性剤の溶解度と表面活性の変化を計算することにより、硬耐性を評価できます。
硬い耐水性を評価する別の方法は、水に分散するために100 gのオレイン酸ナトリウムから形成されたカルシウム石鹸に必要な界面活性剤の割合またはグラムを計算することです。高硬水が高い地域では、高濃度のカルシウムおよびマグネシウムイオンとミネラル含有量がいくつかの実用的な用途を困難にする可能性があります。多くの場合、ナトリウムイオンは合成アニオン性界面活性剤の対イオンとして使用されます。二価カルシウムイオンは両方の界面活性剤分子に結合しているため、界面活性剤が溶液からより容易に沈殿し、洗剤が緩やかになります。
AASの硬い耐水性の研究は、酸と硬い耐水性が追加のカルボキシル基の影響を強く受けていることを示し、2つのカルボン群間のスペーサー基の長さの増加とともに、酸と硬耐性耐性がさらに増加したことが示されました。酸の順序と硬耐性耐性はC 12グリシネート<C 12アスパラギン酸<C 12グルタミン酸でした。ジカルボキシル化アミド結合とジカルボキシル化アミノ界面活性剤をそれぞれ比較すると、後者のpH範囲がより広く、適切な量の酸の添加とともに表面活性が増加することがわかりました。ジカルボキシル化N-アルキルアミノ酸は、カルシウムイオンの存在下でキレート効果を示し、C 12アスパラギン酸は白いゲルを形成しました。 C 12グルタミン酸は、高Ca 2+濃度で高い表面活性を示し、海水淡水化に使用されると予想されます。
6.11分散性
分散性とは、溶液中の界面活性剤の合体と沈降を防ぐ界面活性剤の能力を指します。分散性は、界面活性剤の重要な特性であり、界面活性剤、化粧品、医薬品での使用に適しています。分散剤には、疎水性群と末端疎水グループ(またはまっすぐな鎖疎水性グループ)の間にエステル、エーテル、アミド、またはアミノ結合が含まれている必要があります。
一般的に、アルカノラミド硫酸塩などのアニオン性界面活性剤やアミドスルホベタインなどの両性界面活性剤は、カルシウム石鹸の分散剤として特に効果的です。
多くの研究努力により、N-Lauroyl Lysineは水との互換性が低く、化粧品の使用が困難であることがわかったAASの分散性を決定しました。このシリーズでは、N-アシル置換された塩基性アミノ酸は優れた分散性を備えており、化粧品を改善するために化粧品業界で使用されています。
07毒性
従来の界面活性剤、特にカチオン性界面活性剤は、水生生物に対して非常に毒性があります。それらの急性毒性は、細胞水界面での界面活性剤の吸着イオン相互作用の現象によるものです。界面活性剤のCMCを減らすと、通常、界面活性剤の界面吸着が強くなり、通常、急性毒性が上昇します。界面活性剤の疎水性鎖の長さの増加は、界面活性剤の急性毒性の増加にもつながります。ほとんどのAAは、人間や環境(特に海洋生物)に対して低いまたは非毒性があり、食品成分、医薬品、化粧品としての使用に適しています。多くの研究者は、アミノ酸界面活性剤が穏やかで皮膚に刺激性がないことを実証しています。アルギニンベースの界面活性剤は、従来の対応物よりも毒性が低いことが知られています。
Brito et al。アミノ酸ベースの両親媒性物質の物理化学的および毒物学的特性と、[チロシン(Tyr)、ヒドロキシプロリン(Hyp)、セリン(Ser)、リジン(Lys)]の[誘導体(Lys(Lys))の自発的形成を研究し、カチオン性小胞の自然形成を行い、Dacute Toxicity on Dapnia Magna(IC 50)のデータを提供しました。それらは、臭化ドデシルトリメチルアンモニウム(DTAB)/Lys誘導体および/またはser-/lys誘導体混合物のカチオン性小胞を合成し、それらの生態毒性と溶血の可能性をテストし、すべてのAAとベシクルを含む混合物が従来の界面活性剤DTABよりも毒性が低いことを示しています。
ローザ等。安定したアミノ酸ベースのカチオン性小胞へのDNAの結合(関連)を調査しました。しばしば毒性があるように見える従来のカチオン性界面活性剤とは異なり、カチオン性アミノ酸界面活性剤の相互作用は非毒性であると思われます。カチオン性AAは、特定のアニオン性界面活性剤と組み合わせて安定した小胞を自然に形成するアルギニンに基づいています。アミノ酸ベースの腐食阻害剤も非毒性であると報告されています。これらの界面活性剤は、高純度(最大99%)、低コスト、容易に生分解性、および水性媒体で完全に溶けやすで簡単に合成されます。いくつかの研究では、硫黄含有アミノ酸界面活性剤が腐食阻害において優れていることが示されています。
最近の研究では、Perinelli et al。従来の界面活性剤と比較して、ラムノリピッドの満足のいく毒物学的プロファイルを報告しました。 rhamnolipidsは、透過性エンハンサーとして作用することが知られています。彼らはまた、高分子薬の上皮透過性に対するラムノリピッドの効果を報告しました。
08抗菌活性
界面活性剤の抗菌活性は、最小阻害濃度によって評価できます。アルギニンベースの界面活性剤の抗菌活性が詳細に研究されています。グラム陰性菌は、グラム陽性菌よりもアルギニンベースの界面活性剤に対してより耐性があることがわかりました。界面活性剤の抗菌活性は、通常、アシル鎖内のヒドロキシル、シクロプロパン、または不飽和結合の存在によって増加します。 Castillo et al。アシル鎖の長さと正電荷が分子のHLB値(親水性溶剤バランス)を決定することを示し、これらは膜を破壊する能力に影響を与えることを示しました。 Nα-アシルギニンメチルエステルは、広域抗菌活性を持つカチオン性界面活性剤のもう1つの重要なクラスであり、容易に生分解性であり、毒性が低いか毒性がありません。 Nα-アシルギニンメチルエステルベースの界面活性剤と1,2-ジパリトイル-SN-プロピルトリオキシル-3-ホスホリルコリンと1,2-ジテトラデカノイル-SN-プロピルトリオキシル-3-ホスホリルコリン、モデルメンブレーン、および餌を見せている餌箱での生物を抱えているため、外部の有機物を持っている生物を持っています。抗菌性結果は、界面活性剤が良好な抗菌活性を持っていることを示した。
09レオロジー特性
界面活性剤のレオロジー特性は、食品、医薬品、石油抽出、パーソナルケア、在宅ケア製品など、さまざまな業界でのアプリケーションを決定および予測する上で非常に重要な役割を果たします。アミノ酸界面活性剤の粘弾性とCMCの関係を議論するために、多くの研究が実施されています。
化粧品業界の10のアプリケーション
AASは、多くのパーソナルケア製品の策定に使用されます。カリウムnココイルグリシン酸塩は皮膚に優しいことがわかり、スラッジと化粧を除去するために顔の浄化に使用されます。 N-アシル-L-グルタミン酸には2つのカルボキシル基があり、水溶性が高くなります。これらのAAの中で、C 12脂肪酸に基づくAAは、スラッジと化粧を除去するために顔の浄化に広く使用されています。 C 18鎖を持つAASは、スキンケア製品の乳化剤として使用されており、N-Laurylアラニン塩は、皮膚に刺激されていないため、ベビーケア製品の製剤に使用できるクリーミーなフォームを作成することが知られています。歯磨き粉で使用されるN-LaurylベースのAAは、石鹸と同様の良好な洗剤と強い酵素阻害効果を持っています。
過去数十年にわたり、化粧品、パーソナルケア製品、医薬品のための界面活性剤の選択は、毒性、軽度、触覚と安全性に対する優しさに焦点を当ててきました。これらの製品の消費者は、潜在的な刺激、毒性、環境要因を鋭く認識しています。
今日、AASは、化粧品やパーソナルケア製品の伝統的なカウンターパートよりも多くの利点があるため、多くのシャンプー、ヘア染料、バス石鹸を策定するために使用されています。タンパク質ベースの界面活性剤には、パーソナルケア製品に必要な望ましい特性があります。一部のAAはフィルム形成機能を備えていますが、他のAAには優れた泡の能力があります。
アミノ酸は、角質層で重要な自然発生湿潤因子です。表皮細胞が死ぬと、それらは角質層の一部になり、細胞内タンパク質は徐々にアミノ酸に分解されます。次に、これらのアミノ酸は角質層にさらに輸送され、そこで脂肪または脂肪様の物質をcorne骨層に吸収し、それにより皮膚の表面の弾力性を改善します。皮膚の天然保湿因子の約50%は、アミノ酸とピロリドンで構成されています。
一般的な化粧品成分であるコラーゲンには、肌を柔らかく保つアミノ酸も含まれています。粗さや鈍さなどの皮膚の問題は、主にアミノ酸の不足に起因しています。ある研究では、アミノ酸を軟膏と軟質の燃焼と混合すると、患部がケロイドの傷跡にならずに正常な状態に戻ったことが示されました。
アミノ酸は、損傷したキューティクルの世話に非常に役立つこともわかっています。乾燥した形のない髪は、重度の損傷した角質層のアミノ酸の濃度の減少を示している可能性があります。アミノ酸は、キューティクルを髪のシャフトに浸透させ、皮膚から水分を吸収する能力を持っています。アミノ酸ベースの界面活性剤のこの能力により、シャンプー、髪の染料、髪の柔軟剤、ヘアコンディショナー、およびアミノ酸の存在で非常に便利になります。
日常の化粧品の11のアプリケーション
現在、世界中にアミノ酸ベースの洗剤製剤に対する需要が高まっています。AASは、より良い洗浄能力、発泡能力、布の柔らかい特性を備えていることが知られています。これにより、家庭用洗剤、シャンプー、ボディウォッシュ、その他の用途に適しています。アスパラギン酸由来の両性AAは、キレート特性を伴う非常に効果的な洗剤であると報告されています。 N-アルキル-β-アミノエトキシ酸からなる洗剤成分の使用は、皮膚の刺激を減らすことがわかった。 N-ココイル-β-アミノプロピオン酸からなる液体洗剤製剤は、金属表面上の油染色の効果的な洗剤であることが報告されています。アミノカルボン酸界面活性剤、C 14 Chohch 2 NHCH 2 COONAも、より良い洗剤があることが示されており、テキスタイル、カーペット、髪、ガラスなどの洗浄に使用されています。
n-(n'long-chainアシルβ-アラニル)-β-アラニンに基づく洗剤製剤の調製は、洗浄能力と安定性、イージーフォーム破壊、優れた布の柔らかさのために、KeigoとTatsuyaによって特許の中で報告されています。 KAOは、N-アシル-1 -N-ヒドロキシ-β-アラニンに基づいた洗剤製剤を開発し、皮膚刺激が低いこと、高耐水性、高染色除去能力を報告しました。
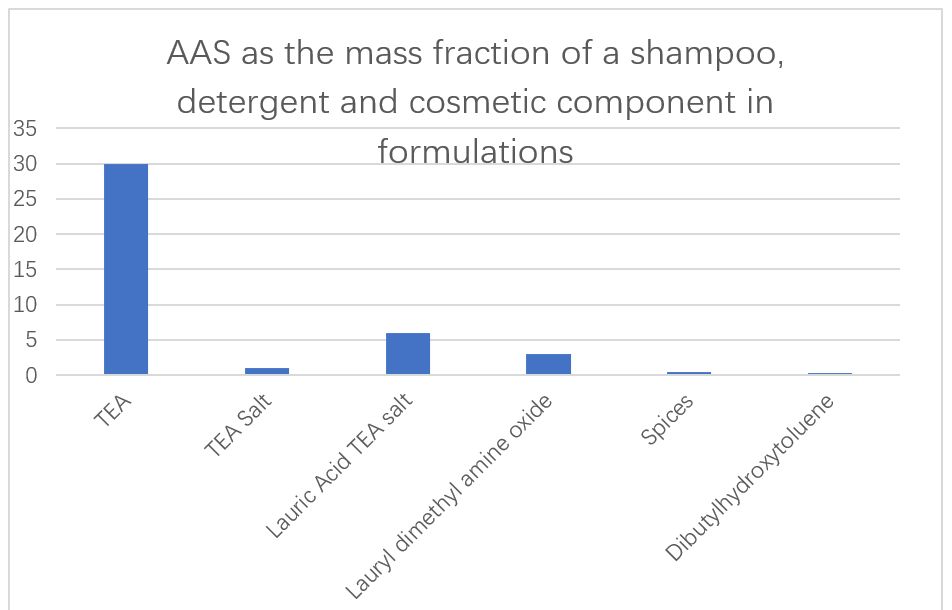
日本企業は、シャンプー、洗剤、化粧品の主な成分として、L-グルタミン酸、L-アルギニン、L-リジンに基づいて、低毒性で簡単に分解可能なAAを使用しています(図13)。タンパク質のファウリングを除去する洗剤製剤における酵素添加剤の能力も報告されています。グルタミン酸、アラニン、メチルグリシン、セリン、アスパラギン酸に由来するN-アシルAAは、水溶液中の優れた液体洗剤として使用するために報告されています。これらの界面活性剤は、非常に低い温度であっても、粘度をまったく増加させず、発泡装置の貯蔵容器から簡単に移して均一なフォームを得ることができます。
投稿時間:2019-2022年6月

